Роль бактерий H pylori в развитии язвенной болезни желудка
Язва желудка и двенадцатиперстной кишки – распространенное заболевание, которым страдают люди от 20 до 65 лет. Мужчины в возрасте от 25 до 40 лет подвержены этому заболеванию в 5-6 раз чаще женщин. Это связано с тем, что мужские половые гормоны повышают кислотность и агрессивность желудочного сока, в то время как женские гормоны снижают их. По данным Всемирной организации здравоохранения, язвенной болезнью страдает от 5 до 10 % населения планеты, и количество пациентов с осложнениями от язвы за последнее десятилетие значительно увеличилось.
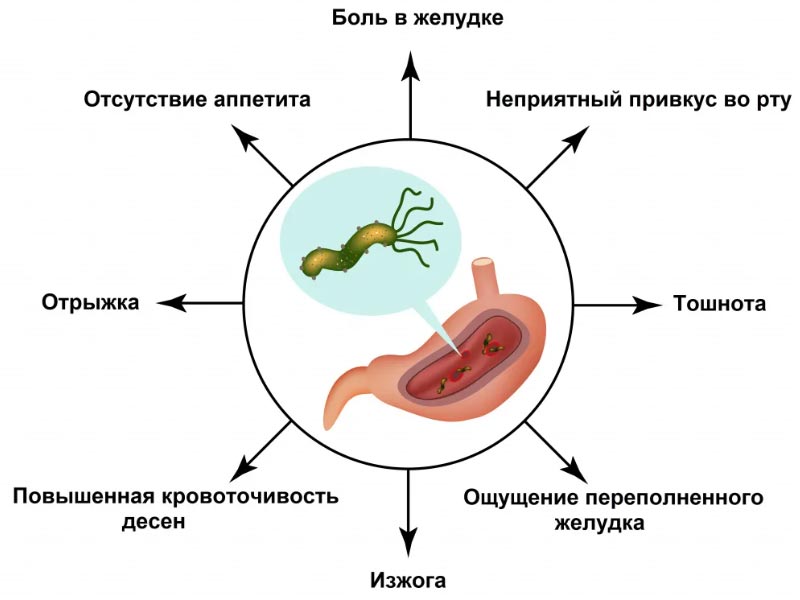
Язвенная болезнь желудка представляет собой долгосрочное рецидивирующее заболевание, характеризующееся наличием язвенных дефектов на слизистой оболочке желудка. Это состояние может быть вызвано несколькими причинами, включая частое употребление алкоголя, физическое перенапряжение, стрессовые ситуации, неправильное питание, употребление острых и соленых блюд, авитаминоз, наличие тромбов в сосудах желудка, а также травмы в области пищеварительной системы.
Способность H. pylori, бактерии, вызывающей гастрит или язву желудка, колонизировать слизистую оболочку желудка зависит не только от состояния иммунитета хозяина, но и от индивидуальных особенностей самой бактерии. Одним из важных факторов её вирулентности является наличие жгутиков, которые обеспечивают быстрое перемещение бактерии в слое густой слизи, защищающей слизистую желудка от кислоты, а также её хемотаксис в местах, где скапливаются другие бактерии того же вида, и быстрая колонизация слизистой.
Липополисахариды и белки наружной оболочки H. pylori имеют способность присоединяться к клеткам слизистой оболочки желудка. Кроме того, липополисахариды наружной оболочки H. pylori вызывают иммунный ответ хозяина и развитие воспаления слизистой.
Выделяемые бактерией во внешнюю среду ферменты, такие как муциназа, протеаза и липаза, вызывают разрушение и растворение защитной слизи, состоящей преимущественно из муцина, и повреждают слизистую желудка.
Очень важную роль во вирулентности H. pylori и его способности выживать в кислой среде желудка играет выделение уреазы — фермента, который разлагает мочевину, образуя аммиак. Аммиак нейтрализует соляную кислоту желудка и поддерживает для бактерий комфортный уровень pH (около 6-7). Одновременно аммиак вызывает химическое раздражение, воспаление и гибель клеток слизистой желудка.
Продукты экзотоксина H. pylori, включая вакуолизирующий экзотоксин, вызывают повреждение и гибель клеток слизистой желудка.
H. pylori обладает специальной «инъекционной системой», которая позволяет инъецировать различные эффекторные белки (включая продукты гена cagA) прямо в клетки слизистой оболочки желудка. Это вызывает воспаление, повышение продукции интерлейкина-8, подавление апоптоза и избыточный рост определенных типов клеток. Полагают, что именно благодаря этим процессам происходит гиперплазия кислотообразующих клеток желудка, гиперсекреция соляной кислоты и пепсина, а в конечном итоге повышается риск развития рака желудка.
Штаммы H. pylori, выделенные от пациентов с язвой желудка или двенадцатиперстной кишки, обычно являются более агрессивными по сравнению со штаммам, выделенными от пациентов с гастритом или от бессимптомных носителей. Как правило, штаммы, выделенные от пациентов с язвенной болезнью, проявляются cagA-положительными (т.е. производят эффекторные белки cagA), а штаммы, выделенные от пациентов с гастритом, чаще продуцируют экзотоксин vacA, чем штаммы, выделенные от бессимптомных носителей.
Патогенетические механизмы
В начальной стадии после попадания в желудок H. pylori быстро передвигается, используя свои жгутики, чтобы преодолеть защитный слой слизи и заселить слизистую оболочку желудка. Когда бактерия прикрепляется к поверхности слизистой оболочки, она начинает вырабатывать уреазу. Этот фермент повышает концентрацию аммиака и увеличивает pH в слизистой оболочке и слое защитной слизи рядом с растущей колонией. Этот процесс вызывает повышенную секрецию гастрина клетками слизистой желудка и компенсаторное увеличение выделения соляной кислоты и пепсина. В то же время, выделение бикарбонатов уменьшается из-за этой отрицательной обратной связи.
Бактерия также вырабатывает муциназу, протеазу и липазу, которые вызывают разложение и растворение защитной слизи желудка. В результате соляная кислота и пепсин получают прямой доступ к обнаженной слизистой оболочке желудка и начинают разъедать ее, вызывая химический ожог, воспаление и образование язвы.
Бактерия также вырабатывает эндотоксин VacA, который вызывает вакуолизацию и гибель клеток эпителия желудка. Продукты гена cagA вызывают дегенерацию клеток эпителия желудка, приводя к изменению их фенотипа (увеличение и удлинение клеток, формирующих так называемый «колибри фенотип»). Различные медиаторы воспаления, вырабатываемые лейкоцитами, привлеченными в результате воспалительного процесса (включая интерлейкин-8, выделенный клетками слизистой оболочки желудка), усиливают воспаление и язвления слизистой оболочки. Бактерия также вызывает окислительный стресс и запускает механизм программированной клеточной смерти эпителиальных клеток желудка.